医药网8月5日讯 8月3日,南京正年夜晴和提交了磷酸专程唑胺片的4类仿造上市,该申请得到CDE承办。早在本年6月,该公司已顺遂提交了打针用磷酸专程唑胺的4类仿造上市申请,今朝相关受理号正在审评审批中。
图1:南京正年夜晴和报告的专程唑胺相关环境
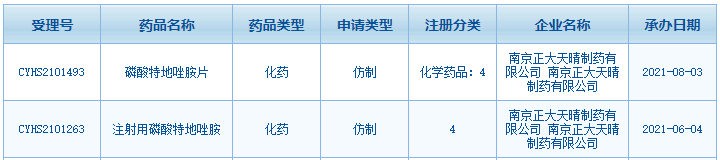
起源:CDE官网
2019年3月,拜耳的磷酸专程唑胺片剂及打针剂得到NMPA同意上市,获批顺应症为革兰氏阳性菌惹起的成人急性皮肤和皮肤组织感化。专程唑胺较第一代恶唑烷酮抗生素利奈唑胺相比次要有两个劣势:一是用法为天天一次共使用六天,比利奈唑胺的天天两次共十天更不便;另一个是剂型有打针剂和片剂,不便临床切换,削减病人住院光阴,从而下降了用度。
图2:今朝专程唑胺报告仿造上市并在审的企业环境
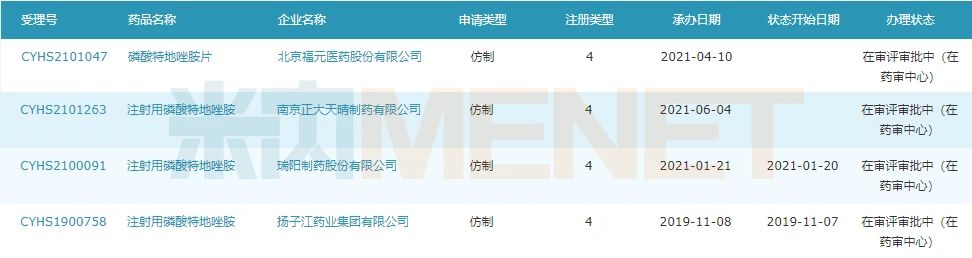
起源:米内网MED2.0中国药品审评数据库
国产仿造药方面,北京福元医药在本年4月提交磷酸专程唑胺片的上市申请,为片剂首家报告企业,南京正年夜晴和为第二家。扬子江在2019年提交了打针用磷酸专程唑胺的上市申请,本年报产的有瑞阳制药和南京正年夜晴和。
从报告光阴来看,南京正年夜晴和均不是首家报告,但剂型是最全的,后续获批上市无望造成合围之势,全力争夺拜耳的市场份额。
数据起源:CDE官网、米内网数据库