郑达天晴创新药疫情今年 17种1类新药来袭
- 2021-12-17 00:00
- 来源:医药资讯网
- 阅读:333
近日,郑达天晴药业有限公司1类新药TQH3910片在国内首次临床申报。米内网数据显示,今年以来,天晴药业共提交上市/临床申请新药22个,其中1类新药17个(首次申请15个)。
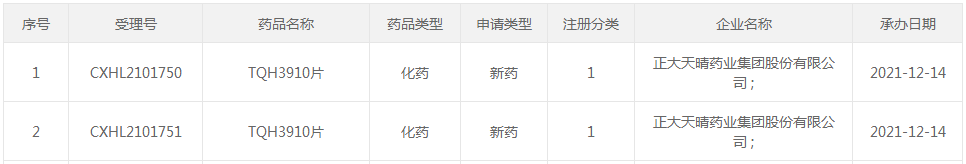
来源:CDE官网
12月14日,郑达天晴药业有限公司提交的TQH3910片作为1类新药的临床申请被CDE受理,受理号为CXHL2101750、CXHL2101751。
经过多年的发展,郑达天晴药业有限公司逐步实现了从“模仿与创造相结合”到“创造与模仿相结合”的提升,创新药物的研发进展迅速。
米内网数据显示,2021年至今,天晴药业共提交新药上市/临床申请(含新适应症)22项,其中生物相似药2项,1类新药17项。从治疗领域来看,anti-肿瘤药物是主要药物。
2021年以来郑达天晴药业提交上市/临床应用的新药
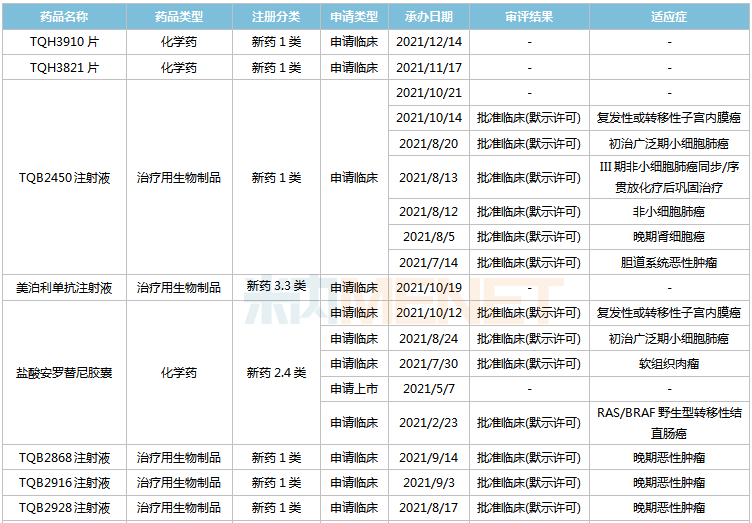
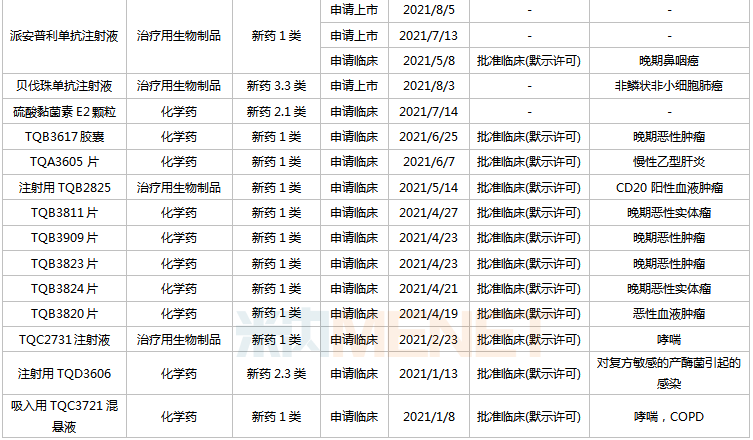
来源:Minenet MED2.0中国药品审评数据库
国内首次临床申报1类新药15个,其中临床获批13个,分别为TQB3617胶囊、TQA3605片、注射用TQB2825片、TQB3811片、TQB3909片、TQB3823片、TQB3824片、TQB3820片、TQC2731注射液、吸入用TQC3721混悬液
在两种生物相似的药物中,据报道贝伐单抗注射液已经开始生产。2021年上半年,该产品在我国公立医疗机构的终端销售额超过30亿元。目前,企业已有8种贝伐单抗生物相似性药物在中国获批。公司率先提交了美吡利注射液的临床应用,2020年原研产品全球销售额达9.94亿英镑。
来源:Minenet数据库、CDE官网等。
注:截至12月15日的数据统计,如有遗漏,请指正!
