长江将拿下抗PE药物大品种 涨幅超100% 增加17亿美元
- 2021-12-08 00:00
- 来源:医药资讯网
- 阅读:71
日前,两种四类仿制药在杨紫茳的上市申请进入行政审批阶段,分别为盐酸鲁拉西酮片(新产品规定)和盐酸达泊西汀片。米内网数据显示,2021H1这两款产品在中国公立医疗机构的销售增长率分别超过800%和100%。
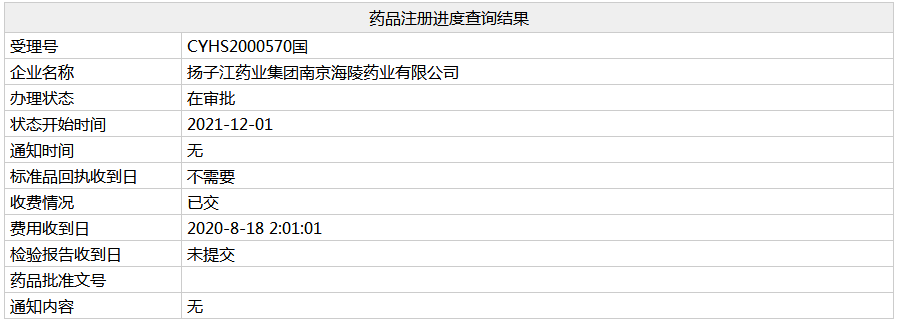
来源:美国食品药品监督管理局官方网站
鲁拉西酮是日本住友制药株式会社研发的新型非典型抗精神病药。鲁拉西酮对5-HT2A受体和多巴胺D2受体都有很高的亲和力,临床上用于精神分裂症和1型双相情感障碍的抑郁发作。该产品于2010年10月获得FDA批准上市,2020年全球销售额为1942亿日元。
原研产品于2019年1月获批进入国内市场,浙江海正药业于2021年4月获得首仿。目前,国内有5家企业公司获得了盐酸鲁拉西酮片的生产许可。内联网数据显示,2021H1年,该产品在中国城市公立医院、县级公立医院、城市社区中心、乡镇卫生院(简称中国公立医疗机构)的终端销售增长率均超过800%。
8家企业提交了新注册分类下的盐酸鲁拉西酮片上市申请。海正药业(40毫克)、郑达天晴(40毫克)、豪森(20毫克、40毫克)和杨紫茳(40毫克)已被批准生产,被视为高估。这一次,长江进入了盐酸鲁拉西酮片,估计20毫克正在审批中。
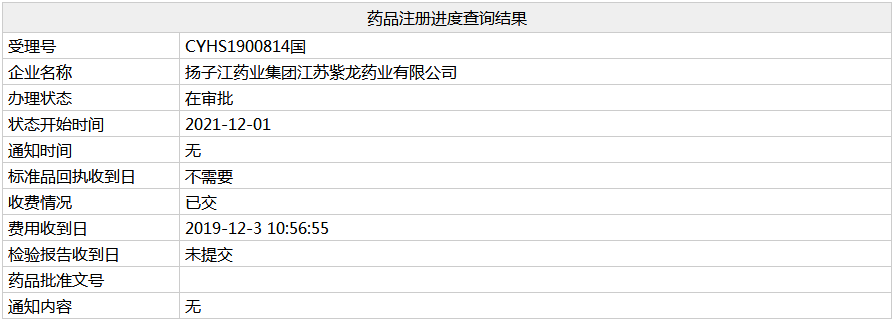
来源:美国食品药品监督管理局官方网站
Paxil是一种选择性5-羟色胺再摄取抑制剂,在男性主要用于治疗18-64岁的早泄(PE)。该产品具有临床效益好、安全风险低、起效快等优点,是《早泄诊治指南》国内外一线治疗药物。
目前国内已有6家企业获得盐酸达泊西汀薄膜生产的批准。根据Minenet的数据,2021H1年该产品在中国公立医疗机构的终端销售增长率超过100%。
11家公司提交了将盐酸达泊西汀薄膜列入新注册类别的申请。科伦、新力泰、山东朗诺、厦门李卓、山东华北凯盛五家公司的产品已获批投产并视同评估,长江冲刺全国第六。
资料来源:Minenet数据库、美国食品药品监督管理局州官方网站等。
注:截至12月7日的数据统计,如有遗漏,请指正!
