国际企业种类瘦身 从药品注册证书刊出看家当变动
医药网6月25日讯 近日,国度药品监视治理局宣布《对于刊出醋酸甲地孕酮疏散片等283个药品注册证书的布告》(以下简称《布告》)。《布告》显示,根据企业申请,国度药监局决议刊出醋酸甲地孕酮疏散片等283个药品注册证书。记者梳剃头现,283个种类除了同质化重大的老普药,还包括部门跨国药企的明星产物。
不丢脸出,跟着仿造药一致性评估推动、药审改造继续深化以及国度药品集中带量推销和使用常态化,国际企业对药品注册证书的意识更为感性,一些药品将跟着注册证的刊出而消逝;与此同时,跨国药企在华运营战略也悄然产生改动,更倾向于将新上市产物以及专利药引入,以避开与中国仿造药的间接竞争。我国医药市场将进一步去赘肉、强筋骨,完成良性倒退。
年夜量药品注册证书“依申请刊出”
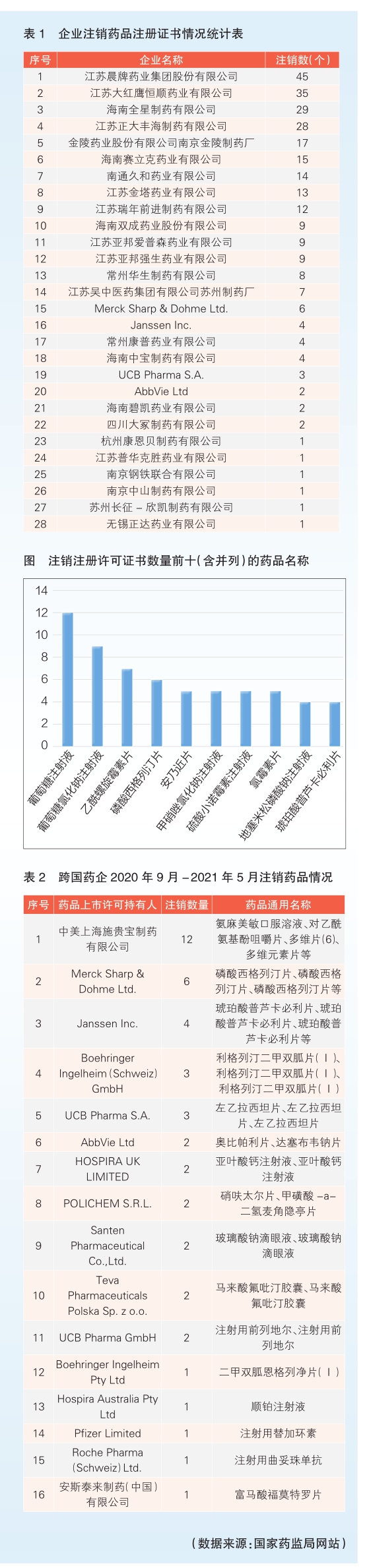
依据《布告》,上述283个药品注册证书波及28家企业,包含24家国际企业和4家跨国药企。此中,刊出药品注册证书数目排名前五(含并列,共12家)的企业别离为江苏晨牌药业集团株式会社、江苏年夜红鹰恒顺药业无限公司、海南全星制药无限公司、江苏正年夜丰海制药无限公司、金陵药业株式会社南京金陵制药厂(见表1)。
梳理国度药监局网站信息,记者发现,包含本次布告在内,自2020年9月以来,国度药监局共宣布五次刊出布告:2020年9月8日,国度药监局布告刊出打针用前列地尔等78个药品注册证书;2020年12月9日,国度药监局布告刊出对乙酰氨基酚片等115个药品注册证书;2020年12月29日,国度药监局布告刊出诺氟沙星胶囊等207个药品注册证书;2021年3月1日,国度药监局布告刊出菠萝卵白酶肠溶片等226个药品注册证书;2021年5月24日,国度药监局布告刊出醋酸甲地孕酮疏散片等283个药品注册证书。这些刊出的药品注册证书绝年夜多半为“依申请刊出”,即企业被动申请刊出的。
相关人士表现,2020年是药品再注册的“年夜年”。依据《药品注册治理方法》,持有人该当在药品注册证书无效期届满前6个月申请再注册。“但每个注册证再注册的用度为近2万元,企业要是有几百个注册证,再注册用度便是几百万元。是以,企业在进行注册证再注册时,会联合企业倒退,权衡本钱与收益,被动放弃部门产物,向省级药监局申请刊出注册证,省级药监局同一报给国度药监局,国度药监局汇总后集中颁布。”
国际企业清算“有效”文号
药品的注册证书是药品的“准生证”。关于企业被动刊出药品注册证,北京百思力营销策动无限公司开创人王恒以为,最间接的起因便是这些种类对企业来说意义不年夜,有的是企业始终未临盆(即业内所称的“僵尸文号”),有的尽管临盆但不挣钱乃至是吃亏,“在某种水平上是国际企业的一种‘断舍离’。”
从通用名来看,《布告》刊出的注册证书中,葡萄糖打针液、葡萄糖氯化钠打针液是刊出数最多的两个种类,别离为12个和9个;此外,乙酰螺旋霉素片、磷酸西格列汀片、安乃近片、甲硝唑氯化钠打针液、硫酸小诺霉素打针液、氯霉素片刊出数均在5个及以上(见图)。
查问国度药监局网站可以发现,这次《布告》刊出的绝年夜多半都是适度反复药品,如葡萄糖打针液、葡萄糖氯化钠打针液现有注册证总数达3300个;乙酰螺旋霉素片现有注册证数目为482个;安乃近片现有注册证数目为844个;甲硝唑氯化钠打针液现有注册证数目为228个;氯霉素片现有注册证数目为354个……种类高度同质化不仅象征着企业很难在市场中盘踞劣势,还象征着仿造药一致性评估压力微小。
依据国度药监局相关布告,在化学药品新注册分类施行前,同意上市的含根本药物种类在内的仿造药,自首家种类通过一致性评估后,其他药品临盆企业的雷同种类准绳上应在3年内实现一致性评估。而实现一个产物的仿造药一致性评估年夜概必要500万元~1000万元。当企业没有才能实现一致性评估时,能做的也只有被动申请刊出该种类的注册证。一位业内子士指出,多年曩昔,药品注册证暗里买卖屡禁不停。但跟着国度鼓舞立异以及医保政策的调整,尤其是在上市允许持有人(MAH)轨制下,药品上市允许让渡出现出新的特色,即充沛考量其临床代价及稀缺性。这也使得企业手中年夜量普药的注册证书失去了让渡(交易)的意义。
跨国药企调整运营战略
值得注意的是,这次《布告》中呈现了跨国药企的明星产物,如艾伯维的奥比帕利片、达塞布韦钠片,默沙东的磷酸西格列汀片、优时比的左乙拉西坦片,杨森的琥珀酸普芦卡必利片等。这并不是跨国药企产物初次呈现在国度药监局刊出药品注册证书布告傍边。据统计,从2020年9月至今,共有16家跨国药企被动刊出了共45个药品注册证书(见表2)。有业内子士以为,跨国药企被动刊出药品注册证,通报出其在华运营战略转变的旌旗灯号。
材料显示,奥比帕利片结合达塞布韦钠片医治方案于2017年9月20日初次在中国获批,于2018年1月上市,用于医治无肝软化或伴代偿期肝软化的基因1型慢性丙肝。记者注意到,今朝,奥比帕利片、达塞布韦钠片在国际尚未有仿造药上市,即艾伯维刊出产物注册证后,这两个产物就此加入中国境内。对此,艾伯维相关人士表现,公司已于2019年上市了全基因型的丙肝医治产物,这次刊出的是第一代产物,只能用于基因1b型医治,且申请刊出是环球同一行为,“在中国境内,留下最好的就行了”。
关于默沙东来说,这次刊出磷酸西格列汀片注册证书能够跟集采政策间接相关。磷酸西格列汀片是一款强效、高选择性的二肽基肽酶-4(DPP-4)克制剂,用于改善2型糖尿病患者的血糖节制。默沙东作为磷酸西格列汀片的原研厂家,这次刊出了旗下波及该产物的6个注册证。
记者在国度药监局网站查问发现,截至6月初,浙江医药、广东东阳光、石药集团欧意药业、正年夜晴和4家公司共有7个品规通过了仿造药一致性评估。显然,磷酸西格列汀片曾经具有进入集采的条件前提。这象征着一旦磷酸西格列汀片被归入集采,默沙东就有能够面对着中国仿造药在价钱上的拼杀。提早刊出药品注册证,象征着选择了提早离场。
有业内子士表现,跨国药企一旦有产物集采中标,要是由于价钱高等起因想要刊出中标产物的注册证,普通不被许可。近日,第五批国度药品集采目次颁布,磷酸西格列汀片尚未被归入。
杨森这次被动刊出的琥珀酸普芦卡必利片是第三批国度药品集采种类,杨森的原研药并未中标(中选的企业别离为石家庄四药、江苏豪森药业、河北仁合益康药业)。地下材料显示,第三批国度药品集采后,杨森在多个省份撤销该产物挂网。
不丢脸出,跟着我国仿造药一致性评估继续推动以及国度药品集采常态化,跨国药企会随之调整运营战略以及产物构造,专利过时的原研药将逐渐加入。
搜索资讯
热门资讯
最新资讯
2025-05-01 16:06:26
2025-05-01 16:06:26
2025-05-01 16:06:26
2025-05-01 16:06:26
2025-05-01 16:06:26
2025-05-01 16:06:26